
小核酸藥物領域開年迎喜訊。
瑞博生物成立于2007年,致力于開發(fā)RNA干擾(RNAi)藥物,目前有8款小核酸藥物進入臨床,在研管線涵蓋了慢性疾病、腫瘤、炎癥、眼科領域,其中5款基于自主研發(fā)的GalNAc(N-乙酰半乳糖胺,目前最常見的偶聯(lián)系統(tǒng))小核酸藥物遞送技術平臺RIBO-GalSTARTM,該平臺高度特異肝靶向具有高效和長效特征。
肝病領域的RBD1016的乙肝和丙肝兩項適應癥分別進入全球臨床的2期和1期。此外,瑞博還有一款靶向Caspases 2視神經保護的siRNA藥物RBD1007,在研適應癥非動脈炎性前部缺血性視神經病變(NAION)已處于臨床3期。
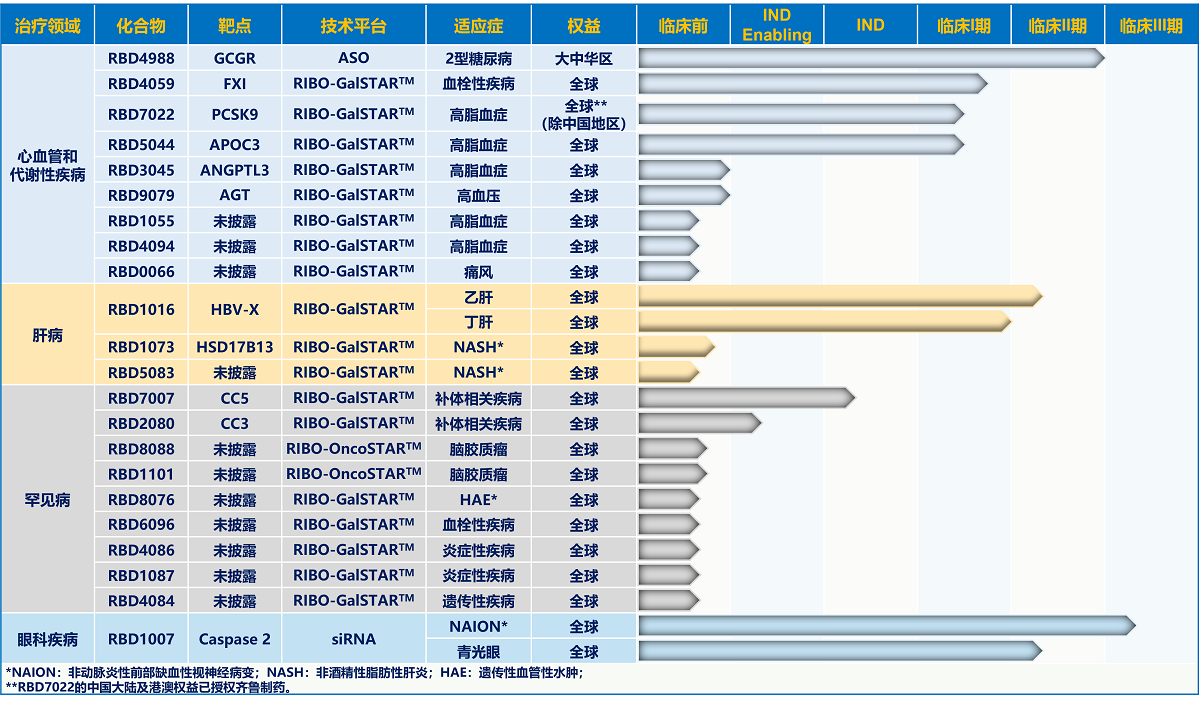
圖1 瑞博生物的在研管線
圖片來源:瑞博生物公司官網
舶望制藥成立于2021年4月,專注于siRNA藥物的開發(fā),成立不到三年來已經建立起多個技術平臺和豐富的研發(fā)管線,在心血管疾病、罕見病、病毒感染、代謝疾病和中樞神經系統(tǒng)疾病領域都建立有產品管線。
心血管領域的BW-01、BW-02已經進入臨床階段,大概率為此次授權諾華的核心產品。根據申報信息,這兩款心血管產品分別用于治療血脂異常和高血壓。
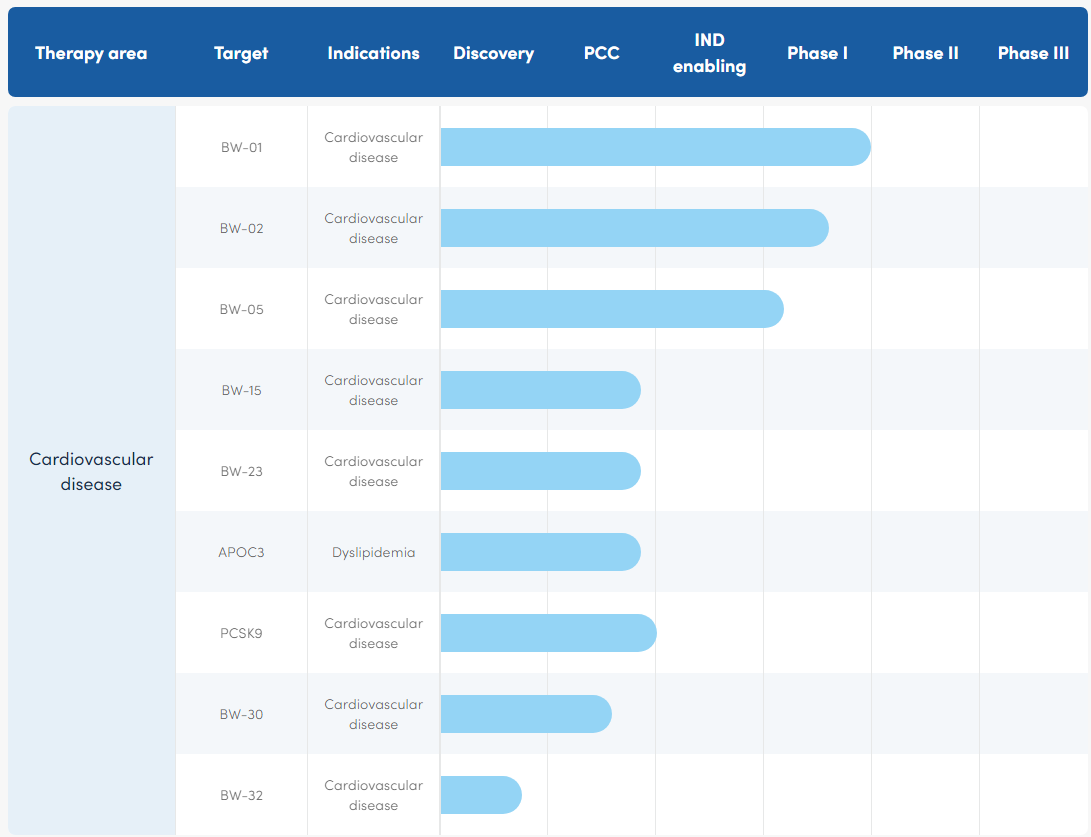
圖2 舶望制藥心血管領域在研管線
圖片來源:舶望制藥公司官網
小核酸藥物的優(yōu)勢
RNA療法主要分為mRNA療法和寡核苷酸藥物(小核酸)兩大類。
小核酸藥物通常為幾十個堿基對長度的單鏈/雙鏈的DNA或RNA,主要通過堿基配對的方式作用于細胞內的mRNA,通過調控蛋白質的表達,實現(xiàn)治療疾病的目的。與傳統(tǒng)化藥,生物藥相比,小核酸藥物具備諸多優(yōu)勢:
RNA能夠與三種主要形式的生物大分子(DNA、RNA和蛋白質)相互作用,所以基于RNA藥物的最大優(yōu)勢之一就是他們能夠靶向細胞內幾乎所有遺傳成分,這使得RNA療法可擴大可成藥靶點的范圍,包括傳統(tǒng)蛋白質和以前未成藥或“不可成藥”的轉錄物和基因。
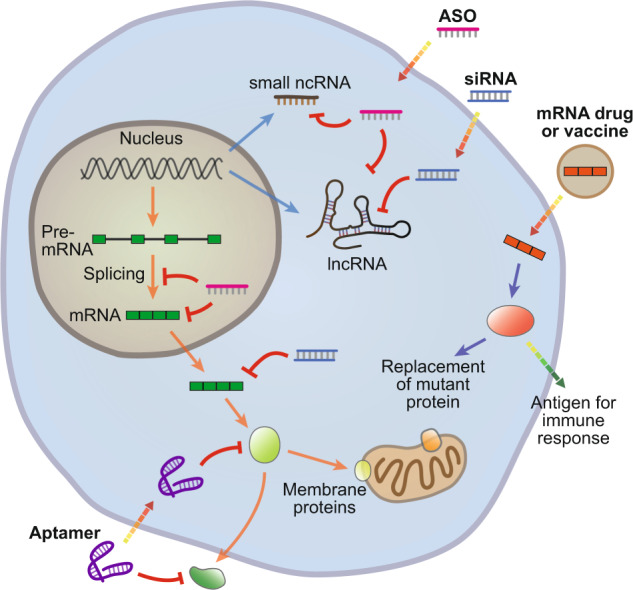
圖3 RNA療法可以靶向多種細胞分子
圖片來源:參考資料3
小分子或者抗體藥物的開發(fā)過程需要數年時間,對RNA藥物一旦確定了RNA的化學結構和進入體內的遞送方式,就可以快速設計和合成基于RNA的藥物用于臨床測試。
天然RNA很容易被核酸酶降解,在對其合成進行各種修飾之后,RNA的穩(wěn)定性大大增加。例如,諾華2021年上市靶向PCSK9的降脂siRNA療法Leqvio,在一次注射后降脂效果可以持續(xù)6個月以上,顯著增加了給藥間隔時間。
由于罕見病藥物的研發(fā)無法保證利潤,因此制藥公司生產治療罕見性疾病的積極性不高。基于RNA藥物而言,一旦RNA的化學性質及其遞送系統(tǒng)得到優(yōu)化,開發(fā)這類藥物的成本就會大大降低。個性化RNA藥物為非常罕見的疾病提供高效治療的可能性。
與基因療法相比,RNA療法沒有顯著的遺傳毒性。在基因療法中,使用病毒載體將DNA分子遞送至細胞,該載體有可能整合到基因組并引起突變,使用RNA可以避免這種潛在風險。
小核酸藥物分子量小、靶點多、半衰期長、生產成本低等優(yōu)勢加持下,使小核酸藥物的研發(fā)成功率更高。以開發(fā)RNA療法的Alnylam公司為例,2012年至2022年間,在公司RNAi平臺下靶向生物標志物的療法中,1期、2期、3期臨床成功率分別為86.7%、81.8%和87.5%,都超過80%,新藥開發(fā)的臨床階段綜合成功率高達62%。
小核酸藥物覺醒
目前已獲批的小核酸藥物按照作用機制大致分為:反義寡核苷酸(ASO)、剪接轉換寡核苷酸(SSO)、RNA干擾(RNAi)和針對蛋白質的RNA適配體,目前小核酸藥物的研究主要集中在ASO和RNA干擾中的siRNA。
截至2023年末,全球已有19款小核酸藥物獲批上市,治療領域主要集中在DMD、罕見的血脂異常、SMA、ALS等罕見病領域。
1998年至2022年全球總共批準了核酸藥物18款,其中3款RNA疫苗獲批上市,其中兩款新冠疫苗COMIRNATY和SPIKEVAX,還有一款乙肝疫苗Heplisav–B,其余15款為小核酸藥物,包括ASO和SSO總計有9款藥物,5款SiRNA藥物,和1款核酸適配體藥物。
其中Vitravene、Macugen和Kynamro已退市,在售產品見圖4。
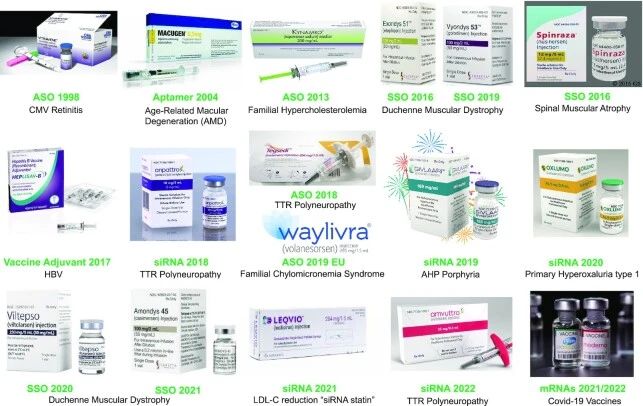
圖4 1998年至2022年批準的小核酸藥物和mRNA疫苗、批準年份以及適應癥
圖片來源:參考資料4
2023年,F(xiàn)DA又批準了4款小核酸藥物上市,分別是渤健/Ionis的TOFERSEN(肌萎縮側索硬化),阿斯利康/Ionis的EPLONTERSEN(多發(fā)性神經病)、諾和諾德的NEDOSIRAN SODIUM(1型原發(fā)性高草酸尿癥)、安斯泰來的AVACINCAPTAD PEGOL SODIUM(年齡性相關性黃斑變性引起的地圖樣萎縮)。
挑戰(zhàn)和發(fā)展并存
小核酸藥物也曾受限于核酸遞送技術,發(fā)展坎坷;2010年前后,由于受限于遞送系統(tǒng),小核酸藥物的研發(fā)屢遭挫折。
2010年羅氏終止在德國和美國的RNAi研究,2011年輝瑞和Abbott砍掉了RNAi藥物研發(fā)項目;2011年MSD關停了舊金山的RNAi藥物研發(fā)中心,2014年將Sirna以1.75億美元的低價賣給Alnylam。2011年,諾華終止了與Alnylam的5年合作關系,2014年大幅縮減RNAi的投入,并停止了波士頓RNAi業(yè)務。
小核酸藥物需要進入人體細胞內發(fā)揮作用,從體外遞送到細胞內這一過程需要克服穩(wěn)定性、免疫原性、跨膜轉運和內吞體逃逸等,即親和力之外,還需要克服化學穩(wěn)定性、對細胞外切和內切核酸酶降解的抵抗力,即代謝穩(wěn)定性、靶位點可及性、遞送和生物分布,與蛋白質和受體的結合、藥代動力學和藥效學以及毒性和補體激活等技術難題。目前主要是通過對核苷酸進行化學修飾來提高底物特異性、增強對核酸酶穩(wěn)定性以及降低免疫原性,修飾的手段包括對核糖、磷酸骨架、堿基以及核酸鏈末端等進行改進。
第一代方法主要是利用硫代磷酸鹽進行主鏈修飾,可通過增加疏水性、對內切酶的抗性等來促進體內細胞攝取、提高生物利用度。
第二代修飾方法是在核糖上2,位的修飾,包括2’-氟、2’-甲氧基等,可以提高對RNA的結合親和力并進一步提升核酸酶抗性。
構象上受限制的DNA類似物鎖核酸和三環(huán)DNA(tcDNA)可以使其具有更強的親和力。
第三代修飾則是核糖的五元環(huán)改造,包括使用PNA、PMO等可以進一步增強核酸藥物對核酸酶的抗性、提高親和力和特異性。
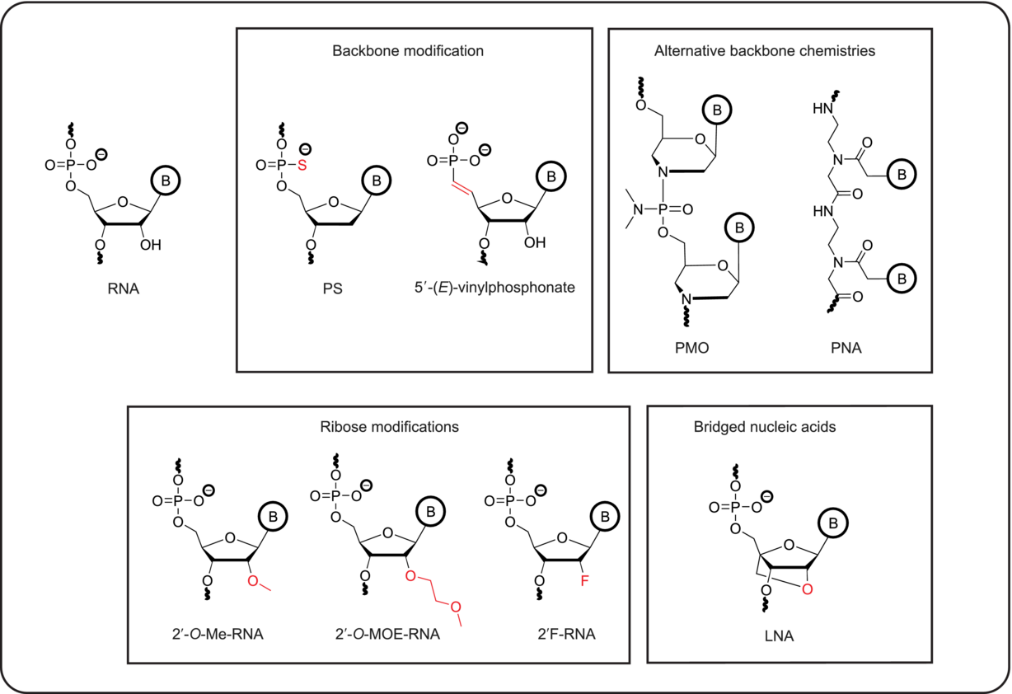
圖5常見的RNA化學修飾
圖片來源:參考資料2
化學修飾可以提高小核酸藥物對核酸酶的抗性、降低免疫原性和增強親和力。但是小核酸藥物需要進入細胞內才能發(fā)揮作用。細胞對小核酸藥物的攝取主要是通過不同類型的內吞作用,小核酸藥物在隨后進入內溶酶體系統(tǒng),需要進行內體逃逸來避免在溶酶體環(huán)境中降解,只有很小部分小核酸藥物能夠逃出內體,并順利發(fā)揮作用。ASO由于分子量相對較小,可能不帶電并有一定的疏水性,可以在不需要遞送劑的情況下有效地進入細胞并逃逸到細胞質和細胞核,不過這時往往需要較高的藥物劑量。對于雙鏈siRNA藥物,由于體積太大,帶負電荷,無法在沒有遞送系統(tǒng)的情況下進入細胞,因此遞送系統(tǒng)的優(yōu)化和改進可以提升小核酸藥物的實用性。
目前的遞送系統(tǒng)有病毒載體和非病毒載體,病毒載體多應用于基因治療,小核酸藥物非病毒載體應用相對更多,非病毒載體又可以分為兩類:與載體直接共軛相連和以納米顆粒載體遞送。
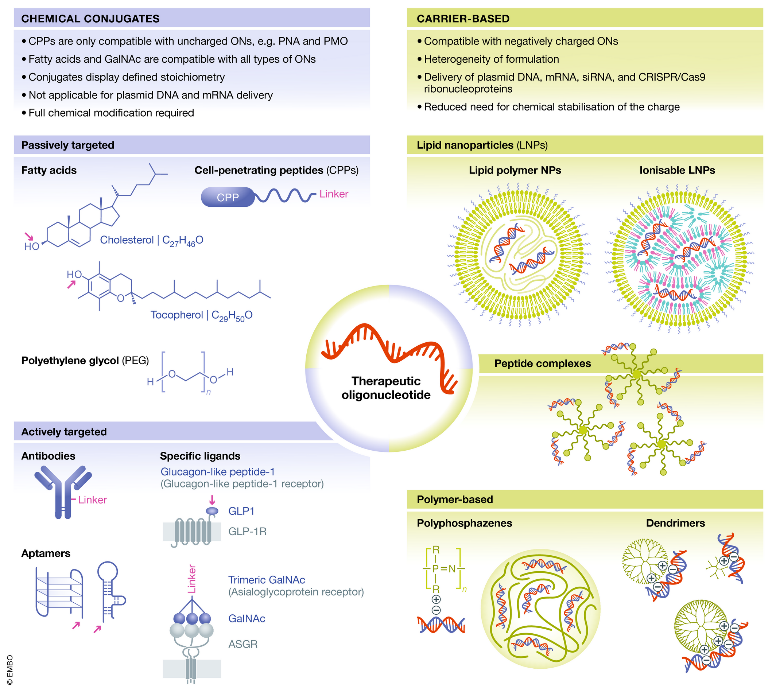
圖6治療性寡核苷酸遞送系統(tǒng),化學綴合物(圖左)和納米顆粒載體(圖右)
圖片來源:參考資料1
聚合物、細胞穿透肽(CPPs)和脂質可以與小核酸藥物共價結合以實現(xiàn)被動靶向,而小核酸藥物與抗體、受體配體和適配體的共價結合則適用于主動靶向。
納米顆粒載體可用于封裝帶負電荷的小核酸藥物,可以基于脂質,如脂質納米顆粒(LNPs)和外泌體;可以基于聚合物,如樹枝狀聚合物和聚磷脂等;也可以基于肽或者由幾種不同類型的化合物組成的混合系統(tǒng)。
CPP只與不帶電的小核酸藥物兼容,如PMO和PAN,脂質體和GalNAc則與所有類型的小核酸藥物兼容。
小 結
小核酸藥物在近幾年取得了長足進步,但是對內吞進入細胞的小核酸藥物來說經過內體逃逸進入細胞質才能發(fā)揮作用,研究表明通過內吞作用的小核酸內體逃逸率不足0.01%。因此解決內體逃逸仍是小核酸藥物遞送中需要解決的問題。此外大多數藥物以肝臟為目標,無特異性地輸送到全身,還需要進一步的技術突破來增強組織特異性遞送;因為大多數的治療針對罕見病,臨床數據有限,隨著高血脂、脂肪肝炎等常見疾病藥物的出現(xiàn),這種情況可能會改變。
展望未來,RNA醫(yī)學領域的發(fā)展,必將會對患者帶來巨大的好處。
參考資料:
文章來源及作者:藥智頭條

 京公網安備 11010802028547號
京公網安備 11010802028547號